FAQ Medikamente Info Austria

1. Welche Register sind in der "Medikamente Info Austria" enthalten?
- Arzneispezialitätenregister
- Vertriebseinschränkungsregister
- Exportverbotsregister
- BASG-Verlautbarung
- BASG-Abstimmung
2. In welchen Sprachen steht die "Medikamente Info Austria" zur Verfügung?
Die “Medikamente Info Austria” kann in den Sprachen Deutsch und Englisch verwendet werden.
3. Wie oft werden die Daten in der "Medikamente Info Austria" aktualisiert?
Die Daten werden einmal täglich aktualisiert. Der Zeitpunkt der letzten Aktualisierung ist in der “Medikamente Info Austria” im Suchbereich ersichtlich.
4. Kann mittels Wildcards gesucht werden?
Ja, Sie können * verwenden, um Ihre Suche in Textfeldern zu optimieren.
Wird *
- vor dem Suchwert angegeben, werden Treffer ausgegeben, in denen der Suchwert irgendwo im Namen vorkommt.
- nach dem Suchwert angegeben, werden Treffer ausgegeben, die mit dem Suchwert beginnen.
- mehrfach verwendet, können Ergebnisse noch spezifischer eingeschränkt und auch als beide Suchmöglichkeiten kombiniert werden.
5. Allgemeines zum Arzneispezialitätenregister
Gesetzliche Grundlage: Verordnung des Bundesministers für Gesundheit über das Arzneispezialitätenregister 2013.
Die Angaben aller in Österreich zugelassenen/registrierten Arzneimitteln können mit Hilfe der “Medikamente Info Austria” abgefragt werden.
Sie können nach mehreren Begriffen suchen und bestimmen damit den Umfang der Ergebnisdaten.
Für Arzneispezialitäten, die zentral zugelassen wurden - erkennbar an der Zulassungsnummer mit EU/.. beginnend -, sind die entsprechenden Informationen auf der Website der EMA (Europäische Arzneimittelagentur) zu finden.
6. Wonach kann ich suchen?
Sie können nach Namen oder Zulassungsnummer suchen. Alternativ steht die Suche nach Wirkstoffen (INN und Synonyme) zur Verfügung.
Weitere Einschränkungen können mit den Suchfeldern im Bereich erweiterte Suche erreicht werden.
7. Welche Daten werden in der Trefferliste des Arzneispezialitätenregisters angezeigt?
- Name: Name der Arzneispezialität gemäß §1 Absatz 4 Ziffer 14 Arzneimittelgesetz (AMG).
- Wirkstoff(e): Arzneilich wirksame Bestandteile gemäß §1 Absatz 4 Ziffer 4a Arzneimittelgesetz (AMG).
- Gebrauchsinformation: Aktuell gültige Gebrauchsinformation (Packungsbeilage) gemäß §16 Arzneimittelgesetz (AMG) (wird nur bei nationalen Zulassungen angezeigt und kann eingesehen/heruntergeladen werden).
- Inhaber:in: Name des/der Inhaber:in der Zulassung/Registrierung/Genehmigung des Parallelimports, gemäß §2 Absatz 13a Arzneimittelgesetz (AMG).
- Rezeptpflichtig: Angabe, ob ein Medikament rezeptpflichtig ist, oder nicht (nähere Informationen zum Rezeptpflichtstatus finden Sie in der Detailansicht des gewählten Medikaments).
8. Welche Daten werden im Reiter "Details" der Detailansicht des Arzneispezialitätenregisters angezeigt?
- Name: Name der Arzneispezialität gemäß §1 Absatz 4 Ziffer 14 Arzneimittelgesetz (AMG).
- Wirkstoff(e): Arzneilich wirksame Bestandteile gemäß §1 Absatz 4 Ziffer 4a Arzneimittelgesetz (AMG). Besitzt ein Arzneimittel mehrere Wirkstoffe werden diese durch das Trennzeichen „I“ getrennt.
- ATC Code: Anatomische-Therapeutische-Chemische Klassifikation gemäß WHO (World Health Organization).
- Rezeptpflichtstatus: Die Rezeptpflicht, ist die Bestimmung, ob ein Arzneimittel von einer Ärzt:in verschrieben werden muss, oder ob es ohne ärztliche Verschreibung (Rezept) in der Apotheke gekauft werden kann. Rechtliche Grundlagen in der jeweils gültigen Fassung: Arzneimittelgesetz (AMG), Rezeptpflichtgesetz, Rezeptpflichtverordnung, Psychotropenverordnung, Suchtmittelgesetz und Suchtgiftverordnung.
- Abgabestatus: Abgabebestimmung gemäß § 57 Arzneimittelgesetz (AMG).
- Relevant gemäß Suchtgift VO: Mit Ja gekennzeichnet, wenn mindestens ein Wirkstoff der Suchtgiftverordnung unterliegt.
- Relevant gemäß Psychotropen VO: Mit Ja gekennzeichnet, wenn mindestens ein Wirkstoff der Psychotropenverordnung unterliegt.
- Inhaber:in: Name und Adresse des/der Inhaber:in der Zulassung/Registrierung/der Genehmigung des Parallelimports, gemäß §2 Absatz 13a Arzneimittelgesetz (AMG).
- Darreichungsform: Darreichungsform eines Arzneimittels.
- Stärke: Stärke eines Arzneimittels.
- Einstellung des In-Verkehr-Bringens gemeldet: Mit Ja gekennzeichnet, wenn dem BASG eine vorübergehende oder endgültige Einstellung des In-Verkehr-Bringens gemäß § 21 Absatz 2 Arzneimittelgesetz (AMG) gemeldet wurde.
- MR/DC/CP Nummer: produktbezogene Nummer, die sich aus dem Länderkürzel des Reference Member States, der Domäne (human oder veterinär), der Produktnummer und der Stärkennummer zusammensetzt, z.B. AT/H/1234/001. Bei zentralen Zulassungen wird die EMA „core number“ angezeigt, z.B. EMEA/H/C/xxxxxx.
- Zulassungsnummer: Eindeutige Nummer für das Arzneimittel, die bei Zulassung vergeben wird und zeitlebens ident bleibt. Zulassungsnummern, die mit EU beginnen kennzeichnen zentral zugelassen Arzneimittel.
- Zulassungsdatum: Datum der Erteilung der Zulassung/Registrierung.
- Arzneimittelkategorie: Kategorie eines Arzneimittels.
- Impfstoff: Mit Ja gekennzeichnet, wenn es sich beim Arzneimittel um einen Impfstoff handelt.
- Allergen: Mit Ja gekennzeichnet, wenn es sich beim Arzneimittel um ein Allergenprodukt handelt.
- Zusätzliche Überwachung: Die Europäische Union hat eine Kennzeichnung für Arzneimittel eingeführt, die zusätzlich - also besonders engmaschig - überwacht werden. Diese Arzneimittel sind in der Fachinformation und in der Gebrauchsinformation (früher Packungsbeilage) durch ein auf der Spitze stehendes, schwarzes Dreieck ▼ gekennzeichnet. Siehe auch https://www.basg.gv.at/fuer-unternehmen/zulassung-life-cycle/faq-zulassung-life-cycle/schwarzes-dreieck
- Chargenfreigabepflicht: Einschränkung für die Chargenfreigabepflicht gemäß § 26 Absatz 1 Arzneimittelgesetz (AMG). siehe auch https://www.basg.gv.at/fuer-unternehmen/zulassung-life-cycle/faq-zulassung-life-cycle/chargenfreigabe
- Ausnahme Chargenprüfung: Einschränkung für eine Ausnahme der Chargenfreigabe gemäß § 26 Absatz 4 Arzneimittelgesetz (AMG). siehe auch https://www.basg.gv.at/fuer-unternehmen/zulassung-life-cycle/faq-zulassung-life-cycle/chargenfreigabe
- Zugelassen in Liechtenstein: Arzneispezialität, die gemäß BGBl. III Nr. 126/2010 (Abkommen zwischen der Österreichischen Bundesregierung und der Regierung des Fürstentums Liechtenstein betreffend die automatische Anerkennung von in Österreich zugelassenen bzw. registrierten Arzneimitteln in Liechtenstein).
- EU Datenbanken:
- Dokumente zu zentral zugelassenen Arzneispezialitäten finden Sie auf der Website der Europäischen Kommission.
- Informationen zu vorhandenen Paralleldistributionen können unter https://iris.ema.europa.eu/registerpd/ gesucht werden.
- Weitere Informationen zu Arzneispezialitäten, die im Gegenseitigen Anerkennungsverfahren (MRP) bzw. Dezentralen Zulassungsverfahren (DCP) zugelassen wurden, finden Sie im Mutual Recognition Index (MRI). Geben Sie dort den Wert aus der Spalte MR/DC/CP Nummer in das „Search“-Feld rechts oben ein, z.B AT/H/1234/001. Achtung: keine EMA „core number“ erlaubt.
- Weitere Informationen zu Tierarzneimitteln (Veterinärarzneispezialitäten) finden Sie auch auf der Website der Europäischen Union. - Verwendung: Angabe, ob das Arzneimittel für Menschen oder für Tiere zugelassen wurde.
- Zieltierart: Für Tierarzneimittel wird jeweils angegeben:
- Anwendungsart
- Dosierung
- Zielgewebe
- Wartezeit: <Wartezeit> <Einheit>
- Besonderheit
9. Welche Dokumente werden im Reiter "Dokumente" in der Detailansicht des Arzneispezialitätenregisters angezeigt?
Bei nationalen Zulassungen werden folgende Dokumente aufgelistet und können angezeigt/heruntergeladen werden, sofern sie vorhanden sind:
- Gebrauchsinformation (GI)
- Fachinformation (FI)
- National Public Assessment Report (NPAR)
- Risk Management Plan (RMP Summary)
Gemäß § 27 Arzneimittelgesetz (AMG) werden die Eckdaten der zugelassenen Arzneispezialitäten und die dazugehörigen Dokumente, wie die Fach- und Gebrauchsinformation (FI, GI) veröffentlicht.
Gemäß § 27 (5) Arzneimittelgesetz (AMG) wird das im Zusammenhang mit der Zulassung erstellte Gutachten (National Public Assessment Report, NPAR) nach Entfernung von im Geheimhaltungsinteresse der Partei liegenden Angaben ebenfalls publiziert. Aus nationalen Verfahren entstandene Gutachten werden in deutscher Sprache veröffentlicht.
PARs aus Europäischen Zulassungsverfahren (MR/DC oder zentral) werden in englischer Sprache veröffentlicht.
- Österreich als betroffener Mitgliedsstaat (Concerned Member State, CMS) verlinkt bei dezentralen Verfahren auf den Mutual Recognition Index. Die Pflege dieser Veröffentlichung obliegt dem jeweiligen RMS.
- Im Zentralen Verfahren zugelassene Produkte werden mit der Website der European Medicines Agency, EMA verlinkt. Die Pflege dieser Veröffentlichung obliegt der EMA.
10. Warum sind für zentral zugelassene Produkten keine Gebrauchsinformationen (GI) sowie Fachinformationen (FI) verlinkt?
Die gültigen Gebrauchsinformationen (GI) sowie Fachinformationen (FI) sind in Datenbanken der EMA verfügbar.
Das "Community Register" ist als Hyperlink hinterlegt und verlinkt auf folgende URL: http://ec.europa.eu/health/documents/community-register/html
Dort kann eine entsprechende Suche abgesetzt werden, wenn der Hyperlink nicht direkt auf die Produktseite führt.
Die Gebrauchsinformationen (GI) sowie Fachinformationen (FI) können im Bereich „Annexes“ einzeln in chronologischer Reihenfolge heruntergeladen werden.
11. Können Ergebnisse aus dem Arzneispezialitätenregister exportiert werden?
Anleitung für die BASG Webseite – Öffnen von CSV Dateien aus dem Arzneispezialitätenregister
Beim Herunterladen von Datensätzen aus dem Arzneispezialitätenregister werden die Informationen ausschließlich im CSV Format zur Verfügung gestellt. Da dieses Format keine eigenen Layout oder Formatierungsinformationen enthält, kann es bei einem direkten Öffnen per Doppelklick vorkommen, dass Inhalte in Microsoft Excel nicht korrekt dargestellt werden.
Um eine saubere und strukturierte Ansicht zu gewährleisten, empfiehlt es sich, die Datei über die Datenimportfunktion von Excel zu öffnen.
Hierfür wird zunächst Excel gestartet und im oberen Menü der Bereich „Daten“ gewählt. Über die Funktion „Aus Text/CSV“ kann anschließend die heruntergeladene CSV Datei ausgewählt werden.
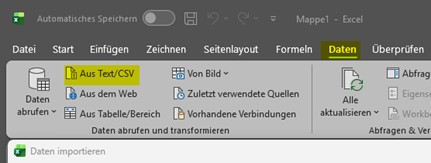
Excel zeigt daraufhin eine Vorschau der Daten an, in der die Erkennungs- und Trennzeichen automatisch richtig zugeordnet werden. Mit einem Klick auf „Laden“ werden die Informationen korrekt in eine Tabelle übernommen. Auf diese Weise lässt sich sicherstellen, dass alle Spalten, Zeichenformate und Datenfelder richtig eingelesen werden – unabhängig von regionalen Einstellungen oder unterschiedlichen CSV Standards.
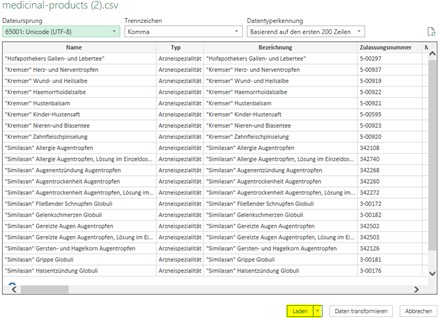
Sollten dennoch Unregelmäßigkeiten auftreten, liegt dies häufig an abweichenden Ländereinstellungen oder daran, dass CSV‑Dateien bei einem direkten Öffnen nicht immer eindeutig interpretiert werden können.
Die Nutzung des beschriebenen Importweges ist daher die zuverlässigste Methode, um vollständige und korrekt strukturierte Daten aus dem Arzneispezialitätenregister in Excel weiterzuverarbeiten.
12. Was ist das "Vertriebseinschränkungsregister" (allgemeines Register)
Im “Vertriebseinschränkungsregister” sind alle gemeldeten Verfahren dargestellt - es handelt sich somit um das allgemeine Register. Meldungen zu verschreibungspflichtigen Arzneispezialitäten werden vor der Veröffentlichung vom BASG überprüft. Nicht enthalten sind Meldungen gemäß § 21 Abs. 2 Arzneimittelgesetz idgF.
Die Meldungen werden ab dem tatsächlichen Beginn der Vertriebseinschränkung automatisch am Folgetag im “Vertriebseinschränkungsregister” veröffentlicht.
Die Verantwortung über die Richtigkeit der Daten liegt bei den Melder:innen. Informationen über vorhandene Bestände in der Verteilerkette (z.B. beim Großhandel, in den Apotheken) liegen dem BASG nicht vor.
13. Wonach kann ich suchen?
Sie können nach Namen oder Zulassungsnummer suchen. Alternativ steht die Suche nach Wirkstoffen (INN und Synonyme) zur Verfügung. Weitere Einschränkungen können mit den Suchfeldern im Bereich erweiterte Suche erreicht werden.
14. Welche Daten werden in der Trefferliste des Vertriebseinschränkungsregister angezeigt?
- Bezeichnung/Name der Arzneispezialität: Name der Arzneispezialität gemäß §1 Absatz 4 Ziffer 14 Arzneimittelgesetz (AMG).
- Wirkstoff(e): Arzneilich wirksame Bestandteile gemäß §1 Absatz 4 Ziffer 4a Arzneimittelgesetz (AMG).
- Status:
- Datum der Meldung:
- Melder:in:
15. Welche Daten werden im Reiter "Vertriebseinschränkung" in der Detailansicht angezeigt?
- Wirkstoff(e): Arzneilich wirksame Bestandteile gemäß §1 Absatz 4 Ziffer 4a Arzneimittelgesetz (AMG).
- Stärke: Stärke eines Arzneimittels.
- Darreichungsform: Darreichungsform eines Arzneimittels.
- Verwendung: Angabe, ob das Arzneimittel für Menschen oder für Tiere zugelassen wurde.
- ATC Code: Anatomische-Therapeutische-Chemische Klassifikation gemäß WHO (World Health Organization).
- Grund
- Zulassungsinhaber:in: Name des/der Inhaber:in der Zulassung/Registrierung/Genehmigung des Parallelimports, gemäß §2 Absatz 13a Arzneimittelgesetz (AMG).
- Zulassungsinhaber:in Kontakt Tel. Nr.
- Zulassungsnummer: Eindeutig Nummer für das Arzneimittel, die bei Zulassung vergeben wird und zeitlebens ident bleibt. Zulassungsnummern, die mit EU beginnen kennzeichnen zentral zugelassen Arzneimittel.
- Hinweis des BASG
- Mitteilung an Fachkreise
- Datum der letzten Änderung
- Datum der Meldung
- Rechtsgrundlage der Meldung
- Exportverbot
- Verfügbarkeit von Packungen
16. Können Ergebnisse aus dem Vertriebseinschränkungsregister exportiert werden?
Anleitung für die BASG Webseite – Öffnen von CSV Dateien aus dem Arzneispezialitätenregister
Beim Herunterladen von Datensätzen aus dem Arzneispezialitätenregister werden die Informationen ausschließlich im CSV Format zur Verfügung gestellt. Da dieses Format keine eigenen Layout oder Formatierungsinformationen enthält, kann es bei einem direkten Öffnen per Doppelklick vorkommen, dass Inhalte in Microsoft Excel nicht korrekt dargestellt werden.
Um eine saubere und strukturierte Ansicht zu gewährleisten, empfiehlt es sich, die Datei über die Datenimportfunktion von Excel zu öffnen.
Hierfür wird zunächst Excel gestartet und im oberen Menü der Bereich „Daten“ gewählt. Über die Funktion „Aus Text/CSV“ kann anschließend die heruntergeladene CSV Datei ausgewählt werden.

Excel zeigt daraufhin eine Vorschau der Daten an, in der die Erkennungs- und Trennzeichen automatisch richtig zugeordnet werden. Mit einem Klick auf „Laden“ werden die Informationen korrekt in eine Tabelle übernommen. Auf diese Weise lässt sich sicherstellen, dass alle Spalten, Zeichenformate und Datenfelder richtig eingelesen werden – unabhängig von regionalen Einstellungen oder unterschiedlichen CSV Standards.

Sollten dennoch Unregelmäßigkeiten auftreten, liegt dies häufig an abweichenden Ländereinstellungen oder daran, dass CSV Dateien bei einem direkten Öffnen nicht immer eindeutig interpretiert werden können.
Die Nutzung des beschriebenen Importweges ist daher die zuverlässigste Methode, um vollständige und korrekt strukturierte Daten aus dem Arzneispezialitätenregister in Excel weiterzuverarbeiten.
17. Was ist das "Exportverbotsregister"?
Das Exportverbotsregister entspricht der „Liste gemäß Verordnung über die Sicherstellung der Arzneimittelversorgung gemäß § 57a Abs. 2 Arzneimittelgesetz“.
Diese Liste basiert auf denselben Daten wie das „Vertriebseinschränkungsregister“, ist jedoch auf jene Arzneispezialitäten eingeschränkt, die nach Überprüfung durch das BASG ein Exportverbot in eine andere Vertragspartei des Europäischen Wirtschaftsraums erhalten haben.
18. Was versteht man unter "Exportverbot"?
Gemäß § 5 Abs. 1 der Verordnung über die Sicherstellung der Arzneimittelversorgung ist aus Gründen des Schutzes der öffentlichen Gesundheit der Export in eine andere Vertragspartei des Europäischen Wirtschaftsraums (EWR) verboten. Ausgenommen davon ist die Ausfuhr für einzelne namentlich bekannte Patient:innen zur unmittelbaren Abwehr einer Lebensbedrohung oder einer schweren gesundheitlichen Schädigung („Named Patient Use“).
Drittstaaten sind vom Exportverbot ausgenommen. Es handelt sich ausschließlich um ein Exportverbot in den EWR, das heißt, dass zum Großhandel Berechtigte mit diesen Arzneispezialitäten keinen Handel aus Österreich in den EWR betreiben.
19. Was ist die Daten- und Rechtsgrundlage für das "Exportverbotsregister"?
Rechtsgrundlage allgemein: Verordnung über die Sicherstellung der Arzneimittelversorgung gemäß § 57a Abs. 2 Arzneimittelgesetz.
Rechtsgrundlage für das Exportverbotsregister: Liste gemäß § 1 Abs. 3 Verordnung über die Sicherstellung der Arzneimittelversorgung, die vom BASG auf seiner Website allgemein zugänglich zu veröffentlichen hat.
Datengrundlage: Nach Überprüfung der Meldung hat das BASG die betreffende Arzneispezialität frühestens am Tag des tatsächlichen Eintritts der Einschränkung der Vertriebsfähigkeit zu veröffentlichen.
20. Welche Daten werden im BASG Verlautbarungsregister angezeigt?
Bescheide des BASG sowie die Änderung einer Arzneispezialität, die für Anwender oder Apotheker von Bedeutung sein kann, werden tagesaktuell veröffentlicht.
Weitere Informationen finden Sie unter: https://www.basg.gv.at/ueber-uns/basg-veroeffentlichungen
21. Wonach kann gesucht werden bzw. die Trefferliste eingeschränkt werden?
- Betrachtungsobjekt (ist der Name eines Arzneimittels) oder Zulassungsnummer (eines Arzneimittels)
- Zeitraum (der Genehmigung)
- in der erweiterten Suche zusätzlich
- ATC Code
- Referenzprodukt
- Inhaber:in
- Klassifizierung
- Verfahrenstyp
- Typ
- Bescheidart
22. Welche Daten werden in der Trefferlister angezeigt?
- Betrachtungsobjekt: ist der Name eines Arzneimittels
- Verfahrenstyp
- Klassifizierung
- Verfahren abgeschlossen am
- Aktuelle Produktinformation
23. Welche Daten werden in den Details angezeigt?
- Name (entspricht Betrachtungsobjekt): Name der Arzneispezialität gemäß §1 Absatz 4 Ziffer 14 Arzneimittelgesetz (AMG)
- Name bisher: bei Änderung des Namens der bisher gültige Name angezeigt
- Zulassungsnummer: Eindeutig Nummer für das Arzneimittel, die bei Zulassung vergeben wird und zeitlebens ident bleibt. Zulassungsnummern, die mit EU beginnen kennzeichnen zentral zugelassen Arzneimittel.
- Verfahrensnummer: technisch eindeutige Nummer des Anbringens
- Verfahrenstyp: Art des Anbringens
- Verfahren abgeschlossen am: Genehmigungsdatum für das Anbringen
- Klassifizierung: Für Änderungsanträge wird gemäß Verordnung (EG) Nr. 1234/2008 der Kommission vom 24. November 2008 über die Prüfung von Änderungen der Zulassungen von Human- und Tierarzneimitteln bzw. § 24 Arzneimittelgesetz (AMG) der Gegenstand der Änderung veröffentlicht.
- Inhaber:in: Name und Adresse des/der Inhaber:in der Zulassung/Registrierung/der Genehmigung des Parallelimports, gemäß §2 Absatz 13a Arzneimittelgesetz (AMG).
- Inhaber:in bisher: bei Änderungen des/der Inhaber:in wird der/die zuvor gültige Inhaber:in angezeigt
- ATC Code: Anatomische-Therapeutische-Chemische Klassifikation gemäß WHO (World Health Organization)
- Rezeptpflichtstatus: Die Rezeptpflicht, ist die Bestimmung, ob ein Arzneimittel von einer Ärztin oder einem Arzt verschrieben werden muss, oder ob es ohne ärztliche Verschreibung (Rezept) in der Apotheke gekauft werden kann.
- Rechtliche Grundlagen in der jeweils gültigen Fassung: Arzneimittelgesetz (AMG), Rezeptpflichtgesetz, Rezeptpflichtverordnung, Psychotropenverordnung, Suchtmittelgesetz und Suchtgiftverordnung.
- Rezeptpflichtstatus bisher: bei Änderungen der Rezeptpflicht wird der zuvor gültige Rezeptpflichtstatus angezeigt
- Referenzprodukt: Referenzarzneimittel gemäß §1 Abs 19 Arzneimittelgesetz (AMG) für generische Arzneimittel
- Typ: Bescheid oder Bescheidberichtigung
- Bescheidart: Grundlage der Entscheidung gemäß Arzneimittelgesetz (AMG)/Tierarzneimittelgesetz (TAMG)
- Ergebnis: Ergebnis der Abstimmung im elektronischen Freigabeprozess
- Genehmigt am: Datum des Abschlusses des elektronischen Freigabeprozesses
- Ablehnender Bescheid: Ablehnung des Anbringens
- Dokumente: akutell gültige Fach- und Gebrauchsinformation als pdf
24. Welche Daten werden im BASG Abstimmungsregister angezeigt?
Nach Entscheidungsfindung werden die Ergebnisse in einem elektronischen Freigabeprozess tagesaktuell aufgelistet.
Weitere Informationen finden Sie unter: https://www.basg.gv.at/ueber-uns/basg-veroeffentlichungen
25. Wonach kann gesucht werden bzw. die Trefferliste eingeschränkt werden?
- Betrachtungsobjekt (kann der Name eines Arzneimittels sein) oder Zulassungsnummer (eines Arzneimittels)
- Zeitraum (der Genehmigung)
- in der erweiterten Suche zusätzlich
- Referenzprodukt
- Inhaber:in
- Verfahrenstyp
- Typ
- Bescheidart
26. Welche Daten werden in der Trefferliste angezeigt?
- Betrachtungsobjekt
- Genehmigt am
- Typ
- Bescheidart
- Inhaber:in
27. Welche Daten werden in den Details angezeigt?
- Betrachtungsobjekt: kann der Name eines Arzneimittels sein
- Verfahrensnummer: technisch eindeutige Nummer des Anbringens
- BASG-Nummer: technisch eindeutige Nummer für den elektronischen Freigabeprozess
- Zulassungsnummer: Eindeutig Nummer für das Arzneimittel, die bei Zulassung vergeben wird und zeitlebens ident bleibt. Zulassungsnummern, die mit EU beginnen kennzeichnen zentral zugelassen Arzneimittel.
- Inhaber:in/Anbringer:in für klin. Prüfung: Name und Adresse des/der Inhaber:in der Zulassung/Registrierung/der Genehmigung des Parallelimports, gemäß §2 Absatz 13a Arzneimittelgesetz (AMG) oder XXX bei CT
- Sponsor: für klinische Prüfungen
- Referenzprodukt: Referenzarzneimittel gemäß §1 Abs 19 Arzneimittelgesetz (AMG) für generische Arzneimittel
- Typ: Bescheid, Nicht-Untersagung, Bescheid (Bescheidberichtigung), Nicht-Untersagung (Bescheidberichtigung)
- Bescheidart: Grundlage der Entscheidung gemäß Arzneimittelgesetz (AMG)/ Tierarzneimittelgesetz (TAMG)
- Ergebnis: Ergebnis der Abstimmung im elektronischen Freigabeprozess
- Genehmigt am: Datum des Abschlusses des elektronischen Freigabeprozesses
- Ablehnender Bescheid: Ablehnung des Anbringens
